Categories: Electricista automòbil
Nombre de visualitzacions: 3345
Comentaris sobre l'article: 0
Què és l’autodescàrrega de la bateria?
Si la bateria no s’utilitza durant algun temps, mantenint el circuit extern obert, pocs dies després podreu trobar que el nivell de tensió dels seus terminals s’ha reduït significativament del que era originalment. Això es deu al fenomen d’autocàrrega - un fenomen normal per a qualsevol bateria, però si l’auto-descàrrega és massa intensa, la norma es converteix en un problema - la capacitat disminueix sensiblement, sense cap raó aparent.
Mirem aquest tema, considerem l’essència i les formes de prevenir aquest tipus de problemes. Convindria considerar el problema de l’autocàrrega mitjançant l’exemple d’una bateria de plom-àcid en un cotxe, perquè qui i els automobilistes saben de primera mà com de vegades pot ser aclaparador si la bateria descarrega simplement mentre es troba en un cotxe bufat en un aparcament o en un garatge, i el seu circuit era obert amb precisió.

Com ja sabeu bateria - Es tracta d’una font de corrent químic, i funciona gràcies als processos químics que es produeixen als elèctrodes i a l’electròlit. A una temperatura més elevada de l'electròlit, els processos es desenvolupen amb més intensitat, a temperatura baixa - menys intensament. I aquest factor de temperatura és important no només durant l’operació, sinó que és rellevant a l’hora d’emmagatzemar la bateria, sempre s’ha de tenir en compte.
D’una manera o altra, l’auto-descàrrega es procedeix segons dos mecanismes: separen l’auto-descàrrega interna de superfície i l’interior. La brutícia, l’aigua i altres líquids presents a la caixa de la bateria formen un circuit molt resistent, aparentment gairebé invisible, tot i que és conductor, al llarg del qual es realitza l’auto-descàrrega superficial. L’auto-descàrrega interna s’associa a reaccions entre elèctrodes i electròlits.

Es produeix una reacció més intensa a l’ànode, l’elèctrode negatiu, on el plom, que interactua amb l’àcid sulfúric, forma una sal (sulfat de plom), mentre que l’hidrogen s’allibera.
Al càtode, l’elèctrode positiu, l’òxid de plom interacciona menys activament amb l’àcid sulfúric, però, també aquí es produeix una reacció de formació de sal amb l’alliberament d’aigua i oxigen. En conseqüència, com més gran sigui la densitat de l'electròlit (més es carrega la bateria) i més alta sigui la temperatura d'emmagatzematge de la bateria, més ràpid es produeix l'auto-descàrrega. La presència d’impureses a l’electròlit també afavoreix l’auto-descàrrega, per tant, com més net sigui l’electròlit, més propera a la normalitat serà l’intensitat d’auto-descàrrega.
Per estimar el valor quantitatiu de l’autocàrrega, primer mesura la capacitat de la bateria C abans de l’emmagatzematge, després espera el temps d’emmagatzematge t, i després mesura la capacitat de la bateria al final del Ct d’emmagatzematge. De manera que troben el valor de l’autocàrrega en un percentatge durant un temps determinat, per exemple, durant un mes o durant un quart. Per a les bateries d’arrencament de plom d’àcid, es considera que el 7% és normal en dues setmanes a una temperatura ambiental de 20 ºC.
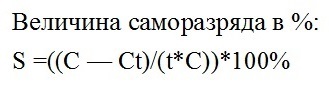
En un esforç per reduir l’auto-descàrrega de les seves bateries, els fabricants de bateries de vehicles estan intentant que els seus elèctrodes puguin evitar reaccions químiques significatives a l’emmagatzematge. Per a aquest propòsit, s’afegeix un dopant, el calci, al plom de l’ànode i s’afegeixen inhibidors a l’electròlit. Busquen evitar les impureses nocives que contribueixen a l’autocàrrega i utilitzen només materials de partida purs.
Pel que fa als automobilistes que volen evitar una descàrrega autònoma forta, els queda mantenir les carcasses de la bateria seques i netes, i per a l'electròlit elaborat per si mateix només s'utilitzi àcid pur i aigua destil·lada.
Consulteu també a electro-ca.tomathouse.com
:
